Resolución N°13 de 08 de enero de 2020
|
Dejar sin efecto el Registro Sanitario 44908, SCHERIPROCT SUPOSITORIOS RECTALES
|
PRIMERO: Dejar sin efecto el Registro Sanitario 44908, correspondiente al producto SCHERIPROCT SUPOSITORIOS RECTALES, elaborado por Bayer De México, S.A. De C.V. de México; Para: Bayer Pharma AG de Alemania.
|
|
08-Enero-2020
|
|
Resolución N°9 de 08 de enero de 2020
|
Dejar sin efecto el Registro Sanitario No. 74662, PANKREOFLAT N TABLETAS RECUBIERTAS
|
PRIMERO: Dejar sin efecto el Registro Sanitario No. 74662, correspondiente al producto PANKREOFLAT N TABLETAS RECUBIERTAS, elaborado por Takeda Mexico, S.A. De C.V .; Para: Bayer Pharma AG de Alemania.
|
|
08-Enero-2020
|
|
Resolución N°10 de 08 de enero de 2020
|
Dejar sin efecto el Registro Sanitario No. 38883, DOMEBORO POLVO
|
PRIMERO: Dejar sin efecto el Registro Sanitario No. 38883 correspondiente al producto DOMEBORO POLVO PARA SOLUCION TOPICA, elaborado por Bayer, S.A., Para: Bayer Pharma AG de Alemania.
|
|
08-Enero-2020
|
|
Resolución N°11 de 08 de enero de 2020
|
Dejar sin efecto el Registro Sanitario No. 85827, ADALAT OROS 30MG
|
PRIMERO: Dejar sin efecto el Registro Sanitario No. 85827, correspondiente al producto ADALAT OROS 30MG COMPRIMIDOS DE LIBERACION OSMOTICA, elaborado por Bayer Pharma AG. Acondicionador: Bayer, S.A. de Guatemala, Para: Bayer AG de Alemania.
|
|
08-Enero-2020
|
|
Resolución N°12 de 08 de enero de 2020
|
Dejar sin efecto el Registro Sanitario 94782, SCHEDERMA CREMA
|
PRIMERO: Dejar sin efecto el Registro Sanitario 94782, correspondiente al producto SCHEDERMA CREMA, elaborado por Bayer De México, S.A. De C.V .; Para: Bayer Pharma AG de Alemania.
|
|
08-Enero-2020
|
|
Resolución N°1 de 07 de enero de 2020
|
Declara Abandonada la solicitud de registro sanitario para el producto DISFLAM 1% GEL TÓPICO
|
Declarar Abandonada la solicitud de registro sanitario para el producto DISFLAM 1% GEL TÓPICO, elaborado por GUTIS LTDA, a la que se le asignó número de trámite 20190587771, solicitado por la Licenciada(o) ROSARIO RODRÍGUEZ CÁCERES, en representación de la empresa PRODUCTOS G.F. DE PANAMA, S.A. -GUTIS FARMACEUTICA.
Por no cumplir con las correcciones u omisiones solicitadas.
|
|
07-Enero-2020
|
|
|
Resol. No. 763 de 28 de diciembre de 2017
|
Principio activo ÁCIDO VALPROICO
|
El Ministerio de Salud de Panamá estableció nuevas disposiciones para la comercialización de medicamentos que contienen Ácido Valproico, debido a riesgos asociados como la teratogenicidad y efectos adversos neurológicos. Esta medida busca proteger la salud pública al garantizar la seguridad y eficacia de este medicamento en el país.
|
|
28-Diciembre-2017
|
|
|
Resol. No. 684 de 16 de noviembre de 2017
|
HIDAMIN (DIFENILHIDANTOINA SODICA) 250 mg/5 mL solución inyectable I.V.
|
Suspender el uso del producto HIDAMIN (DIFENILHIDANTOINA SODICA) 250mg/5mL Solución Inyectable, LV., con Registro Sanitario No. 78728, fabricado por Laboratorios Arsal, S.A. de C.V. de El Salvador.
|
Suspensión de Registro Sanitario
|
16-Noviembre-2017
|
|
|
Resol. No. 220 de 30 de marzo de 2017
|
FENOBARBITAL 0.13g/2ml SOLUCION INYECTABLE I.M
|
SUSPENDER el Registro Sanitario No. 39341 del producto FENOBARBITAL 0.13g/2ml SOLUCION INYECTABLE I.M, Fabricado por Laboratorio Vijosa, S.A., de El Salvador.
|
Suspensión de Registro Sanitario
|
31-Marzo-2017
|
|
|
Resolución N°.010 de 26 de enero de 2015
|
Amitriptilina, clomipramina, dosulepina, doxepina, Imipramina, lofepramina, nortriptilina, citalopram, escitalopram, fluoxetina, fluvoxamina, paroxetina y sertralina.
|
Alerta sobre el riesgo de desarrollar el síndrome de DRESS por el uso de amitriptilina. El DRESS es una reacción alérgica grave que incluye erupciones cutáneas, fiebre e inflamación de órganos internos. Se recomienda a los médicos vigilar estrechamente a los pacientes y suspender el fármaco ante cualquier síntoma sospechoso. Los fabricantes deberán actualizar los prospectos de sus productos para incluir esta advertencia de seguridad.
|
|
26-Diciembre-2015
|
|
|
Resolución N° 571 de 10 de diciembre de 2015
|
PRINCIPIO ACTIVO NIMESULIDA
|
ordena el retiro preventivo del mercado de todos los lotes del medicamento Bravelle (urofolitropina). La medida se basa en una alerta de farmacovigilancia por la pérdida de potencia del fármaco antes de su fecha de vencimiento. Esto podría comprometer la eficacia del tratamiento de fertilidad para el cual se prescribe. Se instruye a las farmacias y distribuidoras a suspender su comercialización de inmediato. La Dirección Nacional de Farmacia y Drogas supervisará el proceso de devolución de las existencias.
|
Cancelación de Registro Sanitario
|
10-Diciembre-2015
|
|
|
Resolución N° 562 de 02 de diciembre de 2015
|
PRINCIPIO ACTIVO FINGOLIMOD
|
ordena actualizar la información de seguridad para los medicamentos con fingolimod. Se exige incluir advertencias sobre el riesgo de desarrollar Leucoencefalopatía Multifocal Progresiva (LMP), una infección cerebral grave. Los médicos deben realizar una resonancia magnética basal antes de iniciar el tratamiento y monitorear síntomas neurológicos sospechosos. La medida aplica a productos innovadores y genéricos, ya sean registros nuevos o vigentes. Se otorga un plazo de seis meses para que los laboratorios realicen estas modificaciones.
|
|
02-Diciembre-2015
|
|
|
Resolución N° 561 de 02 de diciembre de 2015
|
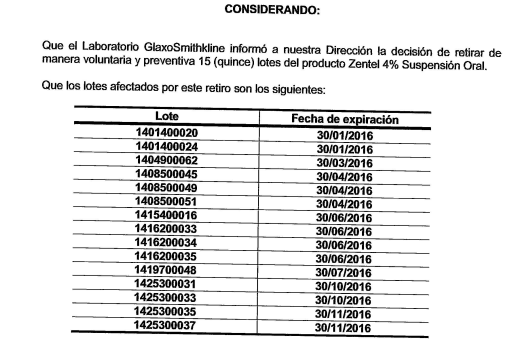
retiro de manera voluntaria y preventiva 15 (quince) lotes del producto Zentel 4%
|
|
|
02-Diciembre-2015
|
|
|
Resolución N° 549 de 25 de noviembre de 2015
|
PRINCIPIO ACTIVO CARISOPRODOL
|
ordena la actualización de la información de seguridad para los medicamentos con carisoprodol. Se exige incluir advertencias sobre el riesgo de dependencia, abuso y somnolencia grave, limitando su uso a periodos cortos. La medida aplica a productos innovadores y genéricos, con un plazo de seis meses para realizar los cambios. El documento busca mitigar riesgos neurológicos y respiratorios asociados al consumo prolongado. Se instruye a los médicos a evaluar cuidadosamente la relación riesgo-beneficio antes de prescribirlo.
|
Cancelación de Registro Sanitario
|
25-Noviembre-2015
|
|
|
Resolución N° 482 de 02 de octubre de 2015
|
MACRODANTINA 50MG CÁPSULAS
|
PRIMERO: Suspender el uso y/o comercialización de los Lotes de Lotes 357881, 455212 y 456918 del producto NTINA SAMG CAPSHLAS MACRODANTINA 50MG CÁPSULAS, con Registro Sanitario No. 71938, fabricado por Bofhringer Ingelheim Tromeco, S.A. de C.V. de México. SEGUNDO: Comunicar a las empresas QUIMIFAR, S.A. y FARMACIA ARROCHA, S.A., distribuidores de dicho a producto, el retiro inmediato del mercado de los Lotes 357881, 455212 y 456918 del producto MACRODANTINA 50MG CAPSULAS, con Registro Sanitario No. 71938, fabricado por Bofhringer Ingelheim Promeco, S.A. de C.V.
|
Suspensión de Registro Sanitario
|
21-Octubre-2015
|
|
|
Resolución N° 521 de 14 de octubre de 2015
|
PRINCIPIO ACTIVO SORAFENIB,SUNITINIB, PAZOPANIB, AXITINIB
|
|
|
14-Octubre-2015
|
|
|
Resolución N° 515 de 13 de octubre de 2015
|
PRINCIPIO ACTIVO CLOPIDOGREL
|
|
|
13-Octubre-2015
|
|
|
Resolución N° 514 de 13 de octubre de 2015
|
PRINCIPIO ACTIVO CRIZOTINIB
|
|
|
13-Octubre-2015
|
|
Resolución N° 513 de 13 de octubre de 2015
|
PRINCIPIO ACTIVO CEFOTAXIMA
|
|
|
13-Octubre-2015
|
|
Resolución N° 512 de 13 de octubre de 2015
|
PRINCIPIO ACTIVO CICLOFOSFAMIDA
|
|
|
13-Octubre-2015
|
|
Resolución N° 511 de 13 de octubre de 2015
|
PRINCIPIO ACTIVO TECNECIO
|
|
|
13-Octubre-2015
|
|
|
Resolución N° 509 de 13 de octubre de 2015
|
PRINCIPIO ACTIVO SEVOFLURANO
|
|
|
13-Octubre-2015
|
|
|
Resolución N° 479 28 de septiembre de 2015
|
PRINCIPIO ACTIVO SITAGLIPTINA
|
|
|
28-Septiembre-2015
|
|
|
Resolución N° 381 de 18 de agosto de 2015
|
Diclofenaco Sodico 75 mg-3 ml solución inyectable i.m. infusión i.v.
|
PRIMERO: PRIMERO: Suspender Suspender elel Kegistro Registro Sanitario Sanitario N° 64238 del producto DICLOFENACO SODICO 75 MG/3 MG/3 MLML SOLUCIÓN SOLUCION INYECTABLE INYECTABLE I.M. I.M. INFUSIÓN I.V. elaborado por VITROFARMA, S.A. DE COLOMBIA; TITULAR VITALIS, S.A.C.I. DE COLOMBIA y distribuido por la empresa VITALIS DE PANAMÁ, S.A. SEGUNDO: Comunicar a la empresa VITALIS DE PANAMÁ, S.A., que deberá retirar del mercado SEGUNDO: Comunicar a ra empresa todos los lotes del producto DICLOFENACO SODICO 75 MG/3 ML SOLUCIÓN INYECTABLE todos fos totes der pr LOTENA e T.M. I.M.
|
Suspensión de Registro Sanitario
|
21-Septiembre-2015
|
|
Resolución 456 de 18 de septiembre de 2015
|
Clobenzorex
|
establece la obligatoriedad de la receta médica para la venta de medicamentos que contienen clobenzorex. La medida se implementa debido a que este fármaco es un estimulante derivado de la anfetamina con riesgo de dependencia y efectos secundarios graves. Se busca prevenir el uso indebido y la automedicación de este producto utilizado principalmente para el tratamiento de la obesidad. El documento instruye a todas las farmacias del país a exigir y retener la prescripción facultativa según corresponda al control de sustancias.
|
Suspensión de Registro Sanitario
|
18-Septiembre-2015
|
|
|
Resolución N° 455 (De viernes 18 de septiembre de 2015)
|
PRINCIPIO ACTIVO PAZOPANIB
|
ordena incluir el riesgo de desprendimiento de retina en la información de seguridad de los medicamentos con pazopanib. La medida aplica a fármacos innovadores y genéricos, ya sean registros nuevos o vigentes. Si la advertencia ya está presente, no es necesario el cambio. Las empresas tienen un plazo de seis meses para realizar la actualización. El objetivo es alertar sobre esta reacción adversa detectada en la monografía e inserto.
|
|
18-Septiembre-2015
|
|
Resolución N° 454 (De viernes 18 de septiembre de 2015)
|
PRINCIPIO ACTIVO CISAPRIDA
|
ordena la cancelación de todos los registros sanitarios de medicamentos con Cisaprida, tanto innovadores como genéricos. La medida se debe a riesgos cardíacos graves, como taquicardia y prolongación del intervalo QT, además de hipertensión pulmonar. Se prohíben nuevas solicitudes, renovaciones y trámites en curso de este principio activo. Los laboratorios fabricantes deben retirar inmediatamente todos sus productos del mercado nacional. La disposición entra en vigor a partir de su publicación oficial para proteger la salud pública.
|
Cancelación de Registro Sanitario
|
18-Septiembre-2015
|
|
|
Resolución N° 453 (De viernes 18 de septiembre de 2015)
|
PRINCIPIO ACTIVO DABIGATRÁN, DRONEDARONA O AMIODARONA
|
ordena actualizar los insertos y monografías de medicamentos con dabigatrán, dronedarona y amiodarona. Se deben incluir advertencias sobre interacciones que aumentan el riesgo de sangrado y ajustar dosis específicas según la patología. No se recomienda el uso de dronedarona junto con dabigatrán por el incremento de su concentración en sangre. La medida rige para productos de marca y genéricos, con un plazo de seis meses para su adecuación. El objetivo es prevenir efectos anticoagulantes excesivos mediante un control clínico estricto.
|
|
18-Septiembre-2015
|
|
Resolución N° 255 de 24 de junio de 2015
|
Montelukast
|
ordena la actualización de la información de seguridad para todos los medicamentos que contienen montelukast. Se exige incluir advertencias destacadas sobre el riesgo de eventos neuropsiquiátricos graves, como agitación, agresión, depresión y pensamientos suicidas. Estos efectos secundarios pueden ocurrir tanto en adultos como en niños, incluso tras dosis iniciales del fármaco. Los profesionales de la salud deben informar a los pacientes y cuidadores sobre estos riesgos y suspender el tratamiento de inmediato si aparecen cambios en el comportamiento.
|
|
24-Julio-2015
|
|
|
Resolución No. 305 de 15 de Julio de 2015
|
Resolución No. 305 de 15 de Julio de 2015
|
establece el Reglamento Sanitario para la comercialización de productos cosméticos en el territorio nacional. El documento define los requisitos técnicos, legales y de etiquetado que deben cumplir las empresas para obtener la notificación sanitaria obligatoria. Se detallan las prohibiciones sobre el uso de sustancias nocivas y las buenas prácticas de manufactura para garantizar la seguridad del consumidor. También regula la vigilancia post-comercialización y los procedimientos de inspección en los establecimientos que distribuyen estos artículos.
|
|
15-Julio-2015
|
|
|
Resolución Ministerial No. 119 de 13 de Julio de 2015
|
Resolución Ministerial No. 119 de 13 de Julio de 2015
|
establece el Reglamento para el Registro Sanitario de Plaguicidas de uso doméstico y de salud pública. El documento define los requisitos técnicos y legales necesarios para la importación, fabricación y comercialización de estos productos en el territorio nacional. Se detallan las normas sobre el etiquetado, almacenamiento y las pruebas de eficacia que deben presentar las empresas interesadas. También se especifican las prohibiciones sobre sustancias químicas altamente tóxicas o persistentes que representen un riesgo inaceptable.
|
|
13-Julio-2015
|
|
Resolución N° 258 de 03 de julio de 2015
|
Teofilin 50mg-5mL Jarabe
|
RIMERO: Considerar abandonada la solicitud de renovación del producto Teofilin 50MG/5ML Jarabe fabricado por Laboratorios Prieto S.A. de Panamá con Registro Sanitario 48855. SEGUNDO: Suspender el uso y comercialización del producto Teofilin 50MG/5ML Jarabe fabricado por Laboratorios Prieto S.A. de Panamá con Registro Sanitario 48855
|
Cancelación de Registro Sanitario
|
11-Julio-2015
|
|
Resolución N° 231 de 25 de mayo de 2015
|
Dife-Nadryl Jarabe
|
Suspender el Registro Sanitario No. 48875, correspondiente al producto correspondiente a prodneto DIFENADRYL 12.5 MG/5ML JARABE, fabricado por LABORATORIOS SAN RAFAEL S.A., DE PANAMA.
|
Suspensión de Registro Sanitario
|
03-Julio-2015
|
|
Resolución N° 243 de 09 de junio de 2015
|
Amoxicilina
|
ordena la actualización de los insertos y fichas técnicas de los medicamentos que contienen amoxicilina solas o en combinación. La medida exige incluir advertencias sobre el riesgo de desarrollar el síndrome de enterocolitis inducida por proteínas alimentarias. Esta es una reacción alérgica gastrointestinal grave que se manifiesta con vómitos prolongados, diarrea, hipotensión y deshidratación severa. Se instruye a los profesionales de la salud a suspender el tratamiento de inmediato si el paciente presenta estos síntomas tras la ingesta del fármaco.
|
|
09-Junio-2015
|
|
Resolución No. 197 de 27 de abril de 2015
|
sobre nuevas disposiciones de seguridad para Ustekinumab
|
ordena la actualización de la información de seguridad para medicamentos que contienen Ustekinumab. Se exige incluir advertencias sobre riesgos cardiovasculares graves, como ataques cardíacos y accidentes cerebrovasculares, detectados en estudios clínicos. También se señala un posible aumento en el riesgo de neoplasias malignas e infecciones graves asociadas al uso de este fármaco biológico. La normativa establece que los pacientes deben ser evaluados regularmente por factores de riesgo cardiovascular antes y durante el tratamiento.
|
|
27-Abril-2015
|
|
|
Resolución No. 184 del 16 de abril del 2015
|
sobre principio activo de Diacereina
|
establece nuevas disposiciones de seguridad para los medicamentos con el principio activo diacereína en Panamá. Se restringe su uso únicamente para el tratamiento sintomático de la artrosis de rodilla y cadera, limitando la dosis inicial a 50 mg diarios durante las primeras semanas para reducir el riesgo de diarrea. El documento contraindica estrictamente su administración en pacientes mayores de 65 años y en aquellos con antecedentes de enfermedad hepática.
|
|
16-Abril-2015
|
|
|
Resolución No. 164 del 6 de abril de 2015
|
sobre principio activo de Leflunomida
|
Ordena modificar la información de seguridad de los medicamentos que contienen leflunomida debido a nuevos riesgos detectados. El cambio principal advierte sobre una cicatrización deficiente de heridas en pacientes que se someten a cirugías mientras están bajo este tratamiento. Se recomienda a los médicos considerar la interrupción del fármaco y realizar un procedimiento de lavado en el periodo periquirúrgico según la evaluación individual del paciente.
|
|
06-Abril-2015
|
|
|
Resolución No. 158 de 31 de marzo de 2015
|
Nuevas disposiciones de seguridad de Vareniclina
|
Ordena el retiro preventivo de todos los lotes de medicamentos que contienen Vareniclina del mercado nacional. La medida se debe a la detección de niveles de N-nitroso-vareniclina por encima de los límites de ingesta diaria aceptables establecidos internacionalmente. Estas impurezas pertenecen al grupo de las nitrosaminas, las cuales están clasificadas como probables carcinógenos en seres humanos tras una exposición prolongada. Se instruye a las farmacias y distribuidoras a suspender la comercialización y proceder con la cuarentena de las existencias actuales.
|
|
31-Marzo-2015
|
|
Resolución No. 156 de 30 de marzo de 2015
|
Nuevas disposiciones de seguridad de codeína
|
Establece nuevas restricciones estrictas para el uso de medicamentos que contienen codeína, especialmente en la población pediátrica. Se prohíbe el uso de codeína como analgésico en menores de 12 años y en menores de 18 años que hayan sido sometidos a cirugías de amígdalas o adenoides debido a riesgos respiratorios graves. La medida responde a casos internacionales de intoxicación por morfina en niños que metabolizan el fármaco de forma ultrarrápida, lo cual puede ser mortal.
|
|
30-Marzo-2015
|
|
|
Resolución N°.033 del 24 de marzo del 2015
|
Se crea el Centro Regional de Farmacovigilancia y Farmacoterapia Región Ngabe Buglé
|
Establece los lineamientos para la implementación de un modelo de atención de salud intercultural en la Comarca Ngäbe-Buglé. El documento busca integrar la medicina tradicional indígena con el sistema de salud pública convencional para mejorar el acceso y la aceptación de los servicios. Se detallan protocolos específicos para el trato digno a los pacientes respetando sus costumbres, lengua y cosmovisión. También incluye la creación de comités técnicos locales que supervisen la aplicación de estas normas en los centros de salud de la región.
|
|
24-Marzo-2015
|
|