Autoridades de Farmacia y Drogas
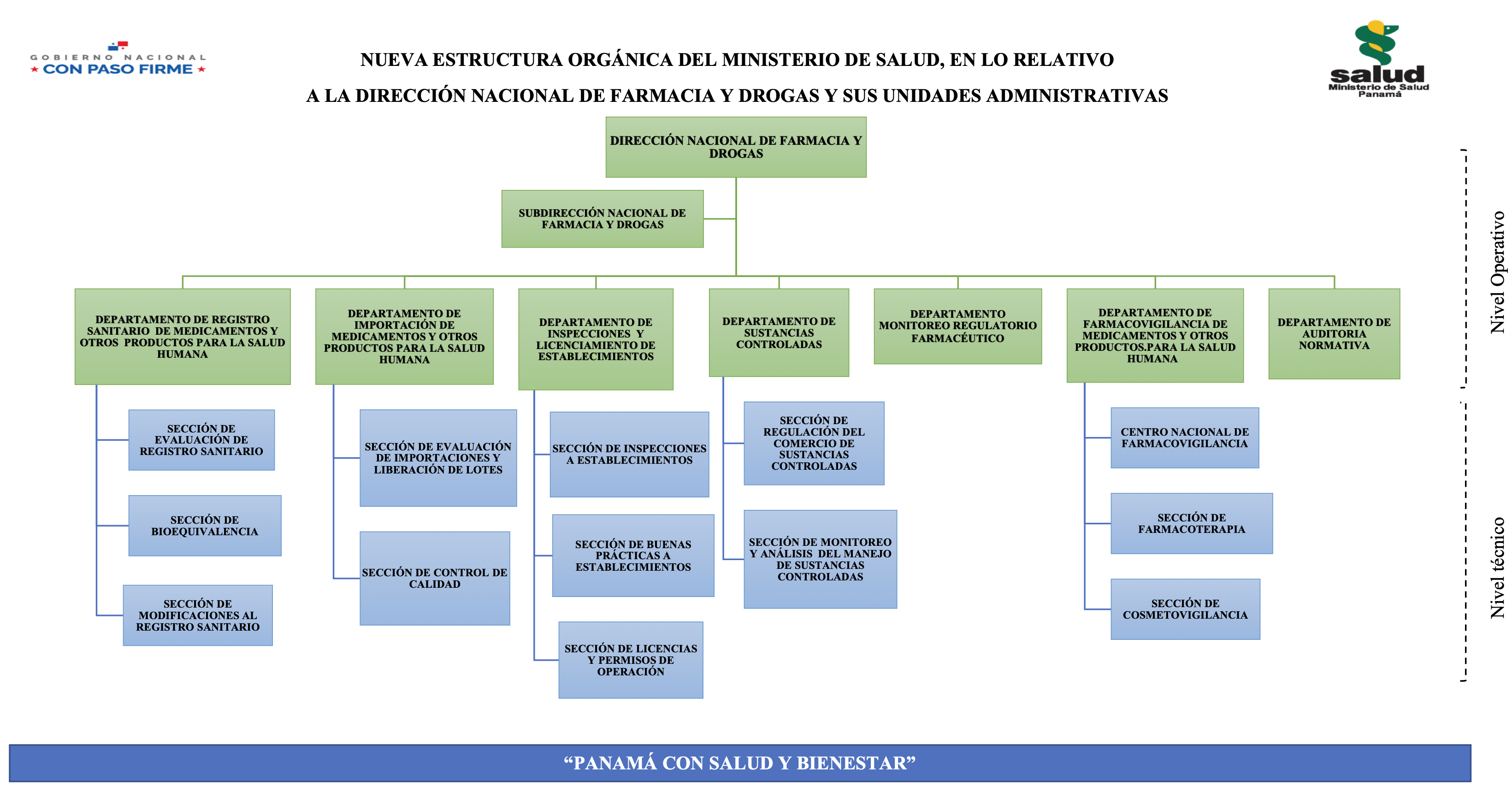
Autoridades por Orden Jerarquico

















Director Nacional de Farmacia y Drogas
Mgter. Uriel B. Pérez M.
Establecer las normas, para el análisis, la vigilancia y el control de calidad de Medicamentos y otros Productos para la Salud Humana, así como las regulaciones de los establecimientos que se dedican a la producción, distribución y custodia de estos, cumpliendo con los estándares de calidad de acuerdo con las legislaciones y reglamentos sanitarios nacionales e internacionales vigentes.

Sub-Directora Nacional de Farmacia y Drogas
Mgter. Alicia M. Castillo M.
Gestionar el cumplimiento de la norma y regulaciones para la vigilancia y el control de calidad de Medicamentos y otros Productos para la Salud Humana, así como las regulaciones de los establecimientos que se dedican a la producción, distribución y custodia de los mismos, cumpliendo con los estándares de calidad de acuerdo con legislaciones y reglamentos sanitarios nacionales e internacionales vigentes.

Administración Farmacia y Drogas
Lcda. Katia Crastz
Coordinar, gestionar y administrar de manera eficiente los aspectos operativos y financieros necesarios para garantizar el óptimo funcionamiento de la Dirección. Participar activamente en la elaboración, presentación y ejecución del Anteproyecto de Presupuesto, así como en la coordinación del Presupuesto de Funcionamiento y Autogestión, asegurando una adecuada planificación de las necesidades a nivel central y departamental. Implementar mecanismos de control presupuestario y contable en estrecha colaboración con la Dirección de Finanzas, manteniendo la transparencia y el uso eficiente de los recursos financieros. Asimismo, supervisar el correcto funcionamiento de la caja de recaudación y la gestión de otros valores asignados a la Dirección Nacional de Farmacia y Drogas.

Departamento de Registro Sanitario de Medicamentos
Lcda. Lorena M.Rojas L.
Verificar el cumplimiento de los procesos de evaluación técnica, conforme a las normas sanitarias vigentes, para expedir el Certificado de Registro Sanitario, el Certificado de Intercambiabilidad y las modificaciones al Registro Sanitario de los medicamentos y otros productos para la salud humana.

Departamento de Importacion de Medicamentos
Lcdo. Tito E. Gonzalez P.
Aprobar los controles de calidad, las importaciones de materia prima, medicamentos y otros productos para la salud humana y la liberación de lotes de productos biológicos mediante la evaluación técnica y/o analítica, para el cumplimiento de la normativa vigente.

Departamento de Inspecciones y Licenciamientos de Establecimientos
Lcda. Ana B. Gonzalez de L.
Regular el cumplimiento de estándares y controles establecidos, mediante inspecciones a establecimientos farmacéuticos y no farmacéuticos, para el otorgamiento de la licencia o permisos de operación, certificados de Buenas Prácticas de Manufactura, Almacenamiento y Distribución, en el marco de las normas sanitarias vigentes.

Departamento de Sustancias Controladas
Lcda. Elsa L. Jara E.
Regular y controlar, el manejo y uso lícito de las sustancias psicotrópicas, estupefacientes, precursores químicos y otras sustancias, basados en las leyes nacionales vigentes y en los Convenios Internacionales, para su uso médico.

Departamento de Monitoreo Regulatorio Farmacéutico
Mgter. Alba G. Arjona M.
Monitorear el progreso de los procesos, fundamentados en una política de gestión de calidad a través de indicadores establecidos y otros métodos de evaluación documentados y aplicados para medir el cumplimiento de estándares establecidos según los procesos regulatorios farmacéuticos dispuestos en las normas vigentes.

Departamento de Auditoría Normativa
Mgter. Jorge J. Alcedo A.
Aplicar las normas y las regulaciones de los establecimientos que se dedican a la producción, distribución, custodia y comercialización, cumpliendo con los estándares de calidad de acuerdo con las legislaciones y reglamentos sanitarios nacionales e internacionales vigentes, para la vigilancia y el control de calidad de Medicamentos y otros Productos para la Salud Humana.

Departamento de Farmacovigilancia
Mgter. Edgar I. Dominguez G.
Establecer estrategias que permita el cumplimiento de lineamientos que procuren el uso racional de los medicamentos, para que la población utilice medicamentos efectivos, mediante el desarrollo de la farmacovigilancia y la farmacoterapia a nivel nacional, y vigilar la seguridad de los cosméticos de acuerdo con la normativa vigente.

Asesoria Legal
Lcda. Liza Lay
Contribuir al cumplimiento de las funciones legales y administrativas de la Dirección mediante la redacción, análisis e interpretación de documentos jurídicos, reglamentos, leyes y resoluciones, asegurando la correcta aplicación del marco normativo vigente. Realizar investigaciones jurídicas y brindar asesoría especializada a las autoridades y funcionarios de los distintos departamentos y secciones, con el propósito de atender, analizar y resolver quejas, denuncias y trámites legales, tanto internos como externos. Asimismo, gestionar de manera eficiente las relaciones legales con entidades públicas y privadas, elaborando informes, notas y recursos jurídicos que respalden la toma de decisiones estratégicas dentro de la institución.